Уравнение Шредингера
Для частиц квантового мира действуют другие законы, чем для объектов классической механики. Согласно предположению де Бройля, микрообъекты обладают свойствами и частицы, и волны – и, действительно, при рассеивании пучка электронов на отверстии наблюдается дифракция, характерная для волн.
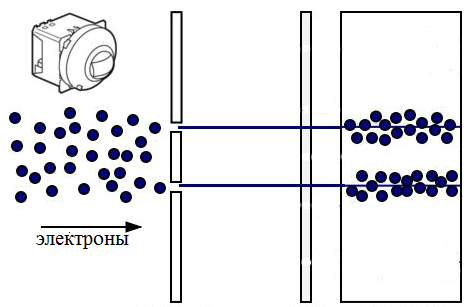
Поэтому можно говорить не о траекториях движения квантовых частиц, а о вероятности того, что частица будет находиться в конкретной точке в некий момент времени.
Что описывает уравнение Шредингера
Уравнение Шрёдингера предназначено для описания особенностей движения квантовых объектов в полях внешних сил. Зачастую частица передвигается сквозь силовое поле, не зависящее от времени. Для этого случая записывается стационарное уравнение Шрёдингера:
В представленном уравнении m и Е – масса и соответственно энергия частицы, пребывающей в силовом поле, а U – потенциальная энергия этого поля. — оператор Лапласа.
— постоянная Планка, равная 6,626•10-34Дж•с.
(её также называют амплитудой вероятности, или пси-функцией) – это и есть функция, позволяющая узнать, в каком месте пространства, скорее всего, будет находиться наш микрообъект. Физический смысл имеет не сама функция, а её квадрат. Вероятность того, что частица находится в элементарном объеме
:
Следовательно, найти функцию в конечном объеме можно с вероятностью:
Так как пси-функция – вероятность, то она не может быть ни меньше нуля, ни превышать единицу. Полная вероятность найти частицу в бесконечном объеме – это условие нормировки:
Для пси-функции работает принцип суперпозиции: если частица или система может находиться в ряде квантовых состояний , то для нее возможно и состояние, определяемое их суммой:
Стационарное уравнение Шрёдингера имеет множество решений, однако при решении следует учесть граничные условия и отобрать только собственные решения – те, которые обладают физическим смыслом. Такие решения существуют только для отдельных значений энергии частицы Е, которые и образуют дискретный энергетический спектр частицы.
Примеры решения задач
ПРИМЕР 1
| Задание | Волновая функция описывает расстояние электрона до ядра водорода: |
| Решение | 1) Выразив объем через радиус ядра, найдем вероятность того, что электрон находится в пределах некоторого расстояния от ядра:
2) Вероятность того, что электрон находится в пределах элементарного «кольца» dr: 3) Чтобы найти наиболее вероятное расстояние, найдем экстремум из последнего выражения: Решив это уравнение, получим r = a – самое вероятное расстояние между электроном и ядром. |
| Ответ | r = a – с наибольшей вероятностью ядро находится на расстоянии первого Боровского радиуса от ядра. |